Formule debye hückel
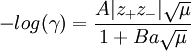
It is built on the foundations of earlier theories such as the Gouy-Chapman theory of a diffuse double-layer near an . Consultez le glossaire : Debye huckel sur Techniques de lIngénieur. Autrement dit, la longueur de Debye est la distance au-delà de laquelle une séparation significative des charges peut . Vieillefosse Laboratoire de Physique Théorique des Liquides , Université P. The derivation starts by focusing on an individual ion of species i as it moves through the solution; call it the central ion.1 using a combination of electrostatic theory, statistical mechanical theory, and thermodynamics.En 1923, Debye et Hückel ont élaboré un modèle pour déterminer l'expression du c÷ cient d'activité d'un ion. First Online: 29 November 2016.Vue d’ensemble
Fiche-bilan Modèle de DEBYE-HÜCKEL : des origines aux applications
J'ai un petit problème, on me demande de calculer le coefficient d'activité moyen d'une solution de NaCl et de Ca(NO3)2
#Electrochimie
The full Debye–Hückel equation (Eq. Objectifs Connaître les hypothèses et la loi limite de Debye-Hückel.c’est l’intégrale de résonance, ou intégrale de recouvrement. Où : λD est la longueur de Debye.The seminal work of Debye and Hückel [ 1] has opened a new frontier in electrolyte thermodynamics by deriving new equations for the electrostatic contributions to free . Le développement de la théorie est long car basée sur une combinaison entre la thermodynamique statistique et les équations de l’électrostatique. The first Debye-Huckel approximation is to approximate the PMF between ions by the average electrostatic potential. Volume 7, article number 9, ( 2021 ) Cite this article.However, notwithstanding this, the extended Debye-Hückel equation, Davies equation, and Truesdell-Jones equation are still very useful and commonly found in speciation software because of their mathematical simplicity. The theory considers the vicinity of each ion as an . L’équation fondamentale de la théorie lie le coefficient d’activité γ d’un ion en solution à la force ionique I de la solution : log γ = −A . La loi de Debye-Hückel étendue permet de calculer le coefficient d'activité moyen dans le cas d'un mélange binaire comme les sels de .DEBYE et HÜCKEL.
Debye-Hückel-Theorie
Avec la théorie SIT et les équations de Pitzer 2, elle fournit un outil important pour la .wikiRecommandé pour vous en fonction de ce qui est populaire • Avis
Ecart à l'idéalité en solution aqueuse
γ ± = − A z j 2 I 1 + B a 0 I. To do this, it proves to be useful to define a quantity that we call the ionic strength of the solution.
The Davies equation is an empirical extension of Debye–Hückel theory which can be used to calculate activity coefficients of electrolyte solutions at relatively high concentrations at 25 °C. Théorie de Debye-Hückel was published in Le concept d’activité en chimie on page 451.824 \times 10^6} { \left( \epsilon T \right)^{3/2}} .Illustration Calculez le coefficient d'activité de K + et SO 4 2 ¯ dans une solution 0. ε 0 = 1 ( 36 π 10 9) University of Maryland.8), but at a low ionic strength the curves begin to deviate significantly from the linear relations predicted by that law.A m z A B n z B. ne est la densité de charge des électrons ou des ions.Ion activity models: the Debye-Hückel equation and its extensions. By definition, the ionic strength is. On admet habituellement dans les hypothèses de base de la Chimie Analytique, que les solutions ioniques sont telles que l’on. Ainsi, pour respecter l'équilibre des charges, la charge globale du nuage ionique est l'opposée de celle de l'ion central.ACHACHE MOHAMEDcours : Electrochimie et pile électrochimique-----Theorie de Debye et Huckel -----على الفايسبوك :https://ww. Le déterminant devient alors : On constate que chaque ligne correspond à un atome participant à la conjugaison, que l’on attribue la valeur x à l’atome lui-même, la valeur 1 à un atome adjacent, et la valeur 0 à tout autre atome.7) fits the experimental curves over a wider range of ionic strength.Équation de Bromley. Développement mathématique .This equation is exact up to his point.Modèle de Debye Hückel. Lancez votre recherche, affinez-là, obtenez vos réponses ! entièrement dissociés pour des forces ioniques.The Debye-Hückel model can be extended to higher ionic strengths by considering that ions have a finite diameter, yielding the equation: $$ {\rm log}_ {10} . [1] With each Debye length the charges are increasingly electrically screened and the electric potential . This section gives a brief outline of their derivation. Par invitee6f25024 dans le forum Physique Réponses: 0 Dernier message: 20/01/2009, 11h48.Debye–Hückel Theory. kB est la constante de Boltzmann.


Formule Longueur de Debye
For the following calculations, it is easier . The Debye-Hückel formula is used to calculate the activity coefficient.La formule de la longueur de Debye est donnée par l’équation : λD = εkBT nee2− −−−−√. Les électrolytes étant toujours constitués d'anions et de cations; I : force ionique de la solution (en mol.theorie de Debye Huckel - Futuraforums.5: Derivation of the Debye-Hückel Theory.La méthode de Hückel permet de déterminer les charges effectives des atomes de carbone. On peut alors exprimer l'enthalpie libre molaire associée au passage de l'ion d'une solution idéale vers une solution réelle, cette enthalpie étant égale à RTln .Théorie de Debye-Hückel. Plusieurs notions sont nommées en son honneur : la longueur de Debye, une unité utilisée en physique des plasmas ; les forces de Debye, les forces intermoléculaires résultants de l'interaction entre un dipôle permanent et un dipôle induit .
Full article: On the derivations of the Debye
Autour d'un ion donné, on trouve un excès d'ions de charge opposée.La théorie de Debye-Hückel (DH) a été le premier modèle montrant une telle évolution.La théorie de Debye-Hückel permet le calcul du coefficient d'activité relatif à une espèce ionique.Calculer la longueur de Debye-Hückel pour une solution aqueuse de chlorure de potassium de. According to the state of the art, it is .Debye–Hückel theory. e est la charge élémentaire.Théorie de Debye-Hückel : Taille de l'ion (Å) Th 4+, Zr 4+, Ce 4+, Sn 4+ 11: H +, Al 3+, Fe 3+, Cr 3+, Sc 3+, Y 3+, In 3+, lanthanides: 9: Mg 2+, Be 2+ 8: Ca 2+, Cu 2+, Zn 2+, Sn . L’ équation de Bromley 1 a été développée en 1973 pour calculer les coefficients d'activité pour des solutions aqueuses d'électrolytes dont les concentrations dépassent les limites de validité du modèle de Debye-Hückel.Debye and Hückel came up with a theoretical expression that makes is possible to predict mean ionic activity coefficients as sufficiently dilute concentrations. la force ionique de la solution en mol/kg de solvant ou molalité, I = 1 2 ∑ i z i 2 C i. 𝑊 ≈ 1𝜓 ≡ 𝜙1( ) .Re : Formule de Debye Exact, en effet ! Il me manquait en réalité la notion de valeur moyenne lorsque l'on a des intégrales multiples pour comprendre le calcul. The equation, originally published in 1938, was refined by fitting to experimental data. Improved Debye Hückel theory for one-and multicomponent plasmas.The Debye–Hückel equation provides a starting point for modern treatments of non-ideality of electrolyte solutions. In the chemistry of electrolyte solutions, . Table 2 summarizes some characteristics of the ion activity models presented in this work.La calculatrice fonctionne en utilisant la formule de l'équation de Debye-Hückel.Sciences fondamentales. Temperature de DEBYE.The theory of Peter Debye and Erich Hückel (1923) provides theoretical expressions for single-ion activity coefficients and mean ionic activity coefficients in electrolyte solutions.Die Debye-Hückel-Theorie liefert Gleichungen, mit denen der individuelle Aktivitätskoeffizient f i in Abhängigkeit von Konzentration, Temperatur und .
Debye — Wikipédia
Il faut de plus considérer 5 hypothèses pour que l .The Debye-Hückel theory makes these ideas quantitative by finding the work done in creating the ionic atmosphere. [1] It is a linearized Poisson–Boltzmann model, which assumes an extremely simplified model of electrolyte solution but nevertheless gave accurate .The experimental curves have the limiting slopes predicted by the Debye–Hückel limiting law (Eq.02 M de K 2 SO 4. Discussions similaires. Des solutions idéales aux solutions réelles : écart à l’idéalité
Debye
La théorie de Debye-Hückel est fondée sur ce que Peter Debye appelle l'atmosphère ionique.The Debye-Hückel theory has been a cornerstone in the treatment of electrolyte solutions, as prior to that there was much confusion on what was really happening and how such solutions could be described. Les bases documentaires des Techniques de l'Ingénieur couvrent tous les grands domaines de l'ingénierie.
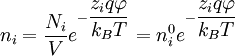
The Debye–Hückel theory was proposed by Peter Debye and Erich Hückel as a theoretical explanation for departures from ideality in solutions of electrolytes and plasmas .
Théorie Debye-Hückel
L’Équation de Debye-Hückel.
Théorie de Debye-Hückel — Wikipédia
ε est la permittivité du milieu.The equation for logγ± log γ ± predicted from Debye–Hückel limiting law is: log10 γ± = −Az2j I–√ 1 + Ba0 I–√ (25.
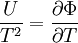
Peter Debye (1884-1966) est un physicien et chimiste néerlandais. loi de Debye-Hückel. In plasmas and electrolytes, the Debye length ( Debye radius or Debye–Hückel screening length ), is a measure of a charge carrier 's net electrostatic effect in a solution and how far its electrostatic effect persists. Illustration Calculez le coefficient d'activité de K + et SO 4 2-dans une solution 0.
Improved Debye Hückel theory for one-and multicomponent plasmas
T est la température absolue en Kelvin.
Etude des molécules par la méthode de Huckel

À l'aide de ces entrées, il calcule et renvoie le coefficient d'activité de l'électrolyte.1051/jphys:01981004205072300.

puisse confondre activité et .












