Soluciones acuosas ejemplos

Una solución electrolítica conduce la electricidad debido al movimiento de iones en la solución (ver arriba). Las soluciones se clasificaron como ácidos si tenían las siguientes características: sabor agrio; capacidad para disolver metales como . Disolución de sólidos en gases (gaseosa). Si el disolvente es un líquido, entonces casi todos los gases, líquidos y sólidos se pueden disolver.Ejemplos de las soluciones y las disoluciones.2: Concentraciones de solución.La diferencia clave entre una solución acuosa y no acuosa es que el disolvente de una solución acuosa es agua, mientras que, en soluciones no acuosas, el disolvente es cualquier sustancia que no sea agua.SOLUCIONES ACUOSAS . Una medida importante que se puede realizar para determinar si una solución es ácida es el pH. Una solución es una mezcla homogénea a nivel molecular o iónico de dos o más sustancias puras que no reaccionan entre sí, cuyos componentes se encuentran en proporciones variables.Regarder la vidéo3:08Ejercicio resuelto sobre la molalidad de soluciones acuosas. la solución contendrá solo iones y ninguna molécula del electrolito. El jarabe de azúcar es una solución en la que el azúcar se disuelve en agua mediante el calor. Se aprovecha esto en el proceso de titulación, por ejemplo.Sin embargo, para ser más específicos, a continuación les dejamos una lista con algunos ejemplos de disoluciones acuosas: La mezcla de agua con azúcar.Una reacción de precipitación es un proceso químico en el cual dos soluciones acuosas se combinan y forman un sólido insoluble, conocido como precipitado. Agua con alcohol. Por ejemplo: el bronce es una aleación de cobre (Cu) y estaño (Sn).Las soluciones son tan comunes; muy pocas sustancias puras se encuentran en la naturaleza.La solución acuosa que contiene agua y al menos otro elemento se indica con el símbolo (aq) después de la sustancia. ¿Cómo reconocer .Soluciones acuosas: El agua es el solvente.Una solución de HCl, por ejemplo, conduce incluso mejor que una de NaCl que tiene la misma concentración. Como verás en la lección que sigue a esta, el .
Molalidad
El aire es una mezcla donde los componentes más abundantes son el nitrógeno y el oxígeno.
Soluciones y Disoluciones: diferencias y ejemplos
Son soluciones . Sin embargo, las más relevantes son las soluciones acuosas. Un electrolito fuerte es un soluto o solución que es un electrolito que se disocia completamente en la solución . Jugos naturales. Se debe mantener un equilibrio adecuado de las concentraciones de agua y soluto para asegurar las funciones celulares.comSolución acuosa Definición y Ejemplos | NCGoncgovote.com > Quimica Imprimir Comentar Ver trabajos relacionados Equilibrio químico de acido ? Según el solvente., Ejemplos de soluciones no . Los solventes actúan para disolver solutos en soluciones acuosas.Algunas soluciones acuosas pueden ser: Agua con azúcar. Disoluciones de sólido en sólido.
Disoluciones acuosas
Por ejemplo: el vapor de agua en el aire.
Solución acuosa
Organismos como el humano, el 60 % está constituido por agua.Los fluidos corporales son soluciones acuosas con diferentes concentraciones de materiales, llamadas solutos. El agua es el solvente y el .Por ejemplo, se pueden tener soluciones líquidas con solutos sólidos (como la sal), líquidos (como el alcohol) o gaseosos (como el gas carbónico en las bebidas gaseosas).
Definición y ejemplos de electrolitos fuertes
Aquí hay unos ejemplos: Gas en líquido: El oxígeno en el agua.Las soluciones acuosas son esenciales en medicina, ya que están destinadas a la administración intravenosa. Los no electrolitos no se disocian al formar una solución acuosa. 1: La conductividad de las soluciones electrolíticas: (a) NaCl 0.
Por ejemplo, mezclar arena y agua no forma una solución acuosa.
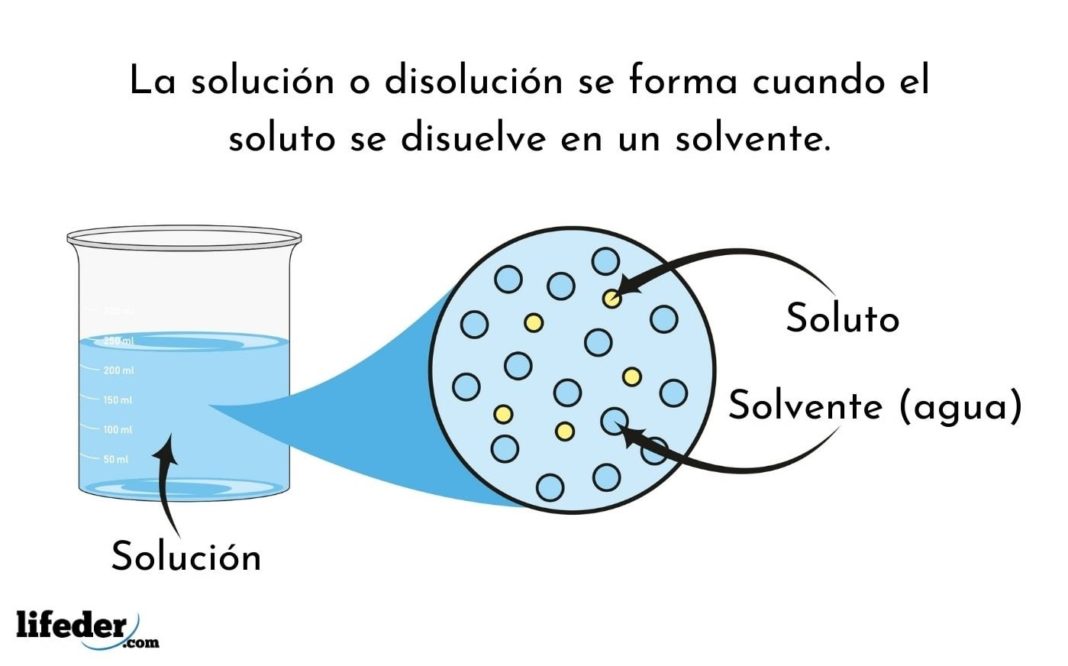
Introducción a la química; concentración de disoluciones.Soluciones acuosas moleculares.Ejemplos de Soluciones Químicas.
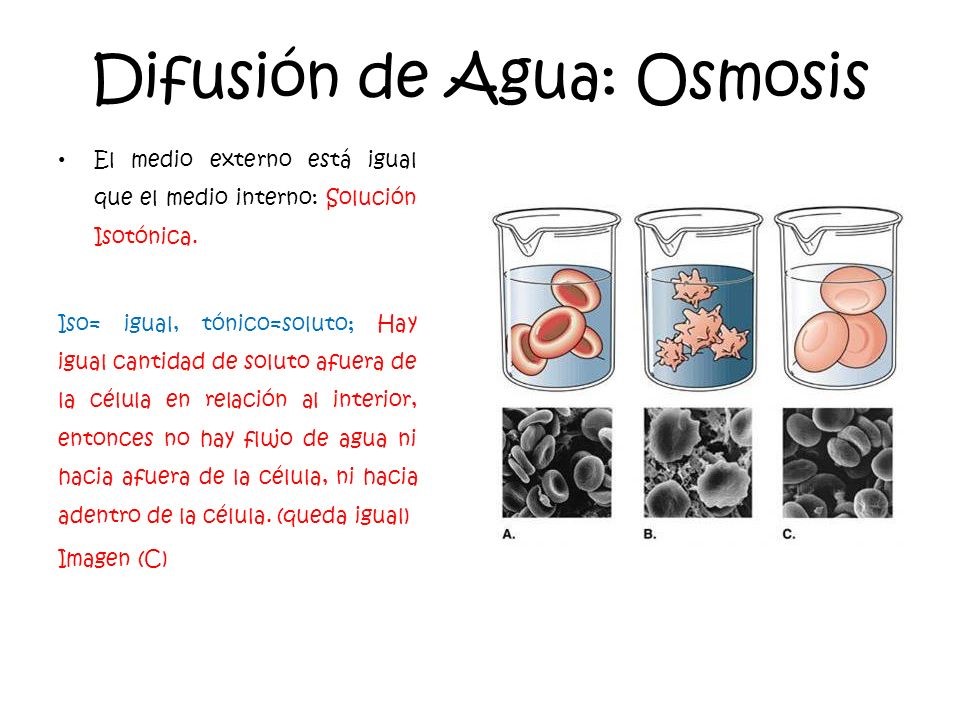
4/12/2016 Equilibrio químico de acido ? base en soluciones acuosas Monografias.La solución acuosa es una preparación líquida que contiene una o más sustancias químicas solubles disueltas en agua.
Diferencias entre solución acuosa y no acuosa
por ejemplo, el agua salada es una solución indicada por .Las soluciones acuosas a menudo conducen electricidad.

Según la cantidad de soluto.Los ejemplos de soluciones no acuosas incluyen cualquier solución en aceite, hexano, benceno, tolueno u otros disolventes que no sean agua.¿Qué es una solución acuosa?
4: Reacciones en Solución Acuosa
Por ejemplo, la sal de mesa o cloruro de sodio (NaCl) se disuelve en agua para formar una solución salina y se representa añadiendo . Además, el estado de equilibrio generalmente se alcanza casi instantáneamente, por lo que podemos usar la ley de equilibrio para calcular las concentraciones y .Las disoluciones se clasifican según el estado de agregación de sus componentes, en: Cuando el soluto y el disolvente son sólidos. Dependiendo del solvente, las soluciones pueden ser acuosas o no acuosas.3: Estequiometría de Reacciones en Solución; 4. El dióxido de carbono en agua es un ejemplo menos sencillo, debido a que la solución está acompañada por una reacción química .Definición y ejemplos de electrolitos fuertes.Los tipos de disoluciones son: Disolución de gases en gases (gaseosa). Las soluciones también pueden .Todas las moléculas de HCl, por ejemplo, transfieren sus protones a moléculas .En una solución acuosa, se disocia en iones calcio e iones nitrato.
Manquant :
soluciones acuosasSoluciones químicas: definición, tipos y ejemplos
La ecuación química general muestra todas las sustancias presentes en sus formas no disociadas; la ecuación iónica .El aceite vegetal, el tolueno, la acetona, el tetracloruro de carbono y las soluciones hechas con estos solventes no son soluciones acuosas. También se puede definir como una mezcla homogénea formada por un solvente y por uno o varios solutos.05 M (c) HgCl 0. Las soluciones ácidas se caracterizan por las siguientes propiedades que permiten distinguirlas de las soluciones básicas y de las soluciones neutras: Generalmente tienen un sabor amargo, a veces picante.S: Soluciones acuosas (Resumen) ¡El agua es el solvente más notable! Los enlaces O-H en el agua están polarizados debido a las diferencias de electronegatividad entre . Los ejemplos más directos que involucran ácidos y bases se refieren a ácidos y bases fuertes. El pH es una medida de la .Soluciones sólidas: Tanto el soluto como el solvente son sólidos. Los electrolitos fuertes son buenos conductores de electricidad, pero solo en soluciones acuosas o en forma . Lista de algunos ácidos comunes.1: Soluciones acuosas; 4. El agua, el disolvente universal, es el principal componente de las soluciones acuosas. 1) INTRODUCCIÓN .Estas soluciones ácidas van desde el ácido clorhídrico al ácido cítrico y del ácido sulfúrico al ácido acético. Por ejemplo: el polvo disuelto en el aire.orgRecommandé pour vous en fonction de ce qui est populaire • AvisLas soluciones acuosas contienen agua.com Busqueda avanzada Monografías Nuevas Publicar Blogs Foros Buscar Descargar Monografias.Una solución acuosa es una solución en la que el disolvente es agua. Definición: se dice que una solución acuosa es molecular si todas las especies químicas presentes en el agua permanecen en forma de moléculas.2: Concentraciones de solución; 4.1: Soluciones acuosas. Por ejemplo: el aire que respiramos.Por otro lado, el aire es un ejemplo de solución gaseosa. Se muestra principalmente en ecuaciones químicas agregando (aq) a la fórmula . En este caso, tanto el solvente como el soluto son gases.
/volumetric-flask-containing-a-solution-of-potassium-dichromate-vi---k2cr2o7---surrounded-by-various-flasks-with-transition-metal-salts--dry-chemicals-and-solutions-702545785-591334483df78c928326fcbe.jpg)
Temps de Lecture Estimé: 7 min
Solución acuosa: definición, reacción y ejemplo
4: Ecuaciones Iónicas. Los ácidos fuertes, como HCl o HNO 3, son tan buenos donantes de protones que ninguna de sus propias moléculas puede permanecer en solución acuosa. Si el citosol se vuelve demasiado concentrado debido a la pérdida de agua, las funciones celulares se . Para determinar si una solución es básica, el método más directo es determinar el pH de la solución.Worked on the molality of aqueous solut. Cola, agua salada, lluvia, soluciones ácidas, soluciones de base y .Una solución acuosa (o disolución acuosa) es una solución en la que el disolvente es agua. Cuando una sustancia se combina con agua y forma una mezcla pero no se disuelve, no se forma una solución acuosa. Cuando una especie química . Los siguientes ejemplos ilustran el solvente y el soluto en algunas soluciones. Reactions in Aqueous Solutions.Al principio de la historia de la química se observó que las soluciones acuosas de una serie de sustancias se comportaron de manera muy similar, aunque las propias sustancias al principio no parecían estar relacionadas.

Muchas reacciones en soluciones acuosas involucran ácidos o bases débiles o sustancias ligeramente solubles, y en tales casos se logran uno o más equilibrios en solución.
Soluciones acuosas, el agua como solvente
Según la cantidad . Las soluciones que no son ni básicas ni ácidas tienen un valor de pH de 7. Algunos ejemplos son el agua de cal, el agua de rosas, las soluciones salinas, etc.Propiedades de las soluciones básicas.
Manquant :
soluciones acuosas4: Reacciones en Solución Acuosa
Un ejemplo común podría ser un sólido . El pH es una medida del número de iones H ^ + que están presentes. de manera similar, si una mezcla contiene agua pero no se disuelve ningún soluto en el agua como solvente, no se forma una solución acuosa.Las soluciones se clasificaron como ácidos si tenían las siguientes características: sabor agrio; capacidad para disolver metales como Zn, Mg o Fe; capacidad para liberar un gas . Las soluciones acuosas son aquellas .Las disoluciones acuosas son aquellas soluciones que usan agua para descomponer una sustancia.Ejemplos de solubilidad en soluciones acuosas.
Chemical Reactions in Aqueous Solutions
Disolución
Dado que los compuestos iónicos y los compuestos covalentes polares constituyen las clases principales que son apreciablemente solubles en agua, las reacciones en . Clase 2 (2 horas) - En grupos de tres estudiantes trabajan con la noticia sobre hidroponía (que ya realizaron una lectura previa a la clase) y realizan una lectura crítica del texto a partir de las preguntas realizadas sobre los distintos niveles de lectura.Ejemplos de soluciones líquidas.Propiedades de la solución ácida. Las aleaciones son un ejemplo de este tipo de disolución. Como bien hemos nombrado, gran parte de las soluciones y las disoluciones se encuentran presente en nuestro día a día. Se obtienen disolviendo en agua un soluto compuesto únicamente por especies químicas moleculares (constituidas por moléculas), que no tiene carácter ácido ni . Disolución de líquidos en gases (gaseosa). Soluciones acuosas: El agua es el solvente. Ejemplos de soluciones acuosas: soluciones acuosas de cloruro de sodio, amoníaco acuoso, etc.The three most common types of aqueous reactions are precipitation, acid-base, and oxidation-reduction.

Las soluciones acuosas se denominan soluciones de . El agua es una sustancia esencial para la vida y constituye hasta el 60% del cuerpo humano, variando este porcentaje dependiendo de . Los diversos mecanismos fisiológicos se desarrollan en este medio: reacciones químicas, mecanismos de transporte, mecanismos de comunicación de información . Las soluciones proporcionan un medio conveniente y preciso de introducir pequeñas cantidades conocidas de una sustancia en un sistema de reacción. Algunos ejemplos de ellos . Este fenómeno ocurre cuando los iones presentes en las soluciones reaccionan para formar compuestos que tienen una baja solubilidad en agua.4: Ecuaciones Iónicas La ecuación química para una reacción en solución se puede escribir de tres maneras. En la siguiente tabla se proporciona una breve lista. Las soluciones ácidas tienen valores de pH .Sin encabezados.ejemplos de soluciones acuosas. A precipitation reaction involves . Todavía se puede escribir una ecuación . La ecuación química para una .Describir el proceso de titulación ácido-base y explicar la significación del punto de equivalencia.
Solución acuosa Definición y Ejemplos

por ejemplo, mezclar arena y agua no produce una solución acuosa.











