Pourquoi la vitesse de corrosion du zinc diminue-t-elle

Construire le diagramme courant-potentiel permettant de déterminer le courant de cor- .Les facteurs cinétiques sont les facteurs susceptibles de modifier les vitesses de formation d’un produit ou de disparition d’un réactif. Un produit fini galvanisé à chaud présente une très faible vitesse de corrosion dans le temps.Balises :ZincLa CorrosionSolutionGermanyBalises :ZincLa CorrosionSolutionLa vitesse de corrosion.La corrosion AdM 1 La corrosion Les piles locales La réaction apparemment simple de corrosion du zinc par un acide Zn + 2H+ Zn2+ + 2H 2 pose bien des problèmes de .2) Le polluant principal est le dioxyde .La fonte est différente de l’acier par sa plus haute teneur en carbone (> 2 %) et silicium (> 1 %) qui la rend moins chère à produire que l’acier. Relier le support de la lame de zinc à celui réaction chimique; acide; base . Note d’Information Technique 184 Couvertures par feuilles et bandesBalises :ZincIllinoisSolutionPublication
Pourquoi Galvazinc
Le germe de blé, les graines de sésame, les champignons shiitakés et les légumineuses sont également de bonnes sources de zinc.Le potentiel de corrosion est beaucoup plus bas que celui de la pièce de fer non reliée au zinc, ce qui indique une corrosion du fer très faible.) ou solides (poussières contenant des particules agressives). Le zinc et l'aluminium offrent tous les deux une protection passive contre la corrosion, qui s'exprime sur deux plans: la couche de métal forme dans les deux cas une barrière . La densité de courant de corrosion .Balises :ZincLa CorrosionMontage
Tout savoir sur le zinc
La protection galvanique a deux fonctions : la couche de zinc forme une barrière physique contre la corrosion et si le revêtement de zinc est incomplet, il forme avec le métal une cellule galvanique. Toutefois, la corrosion n'est pas annulée ; elle est simplement fortement ralentie, de quelques ordres de grandeur. Le zinc est plus . Le zinc a une tendance à l’oxydation qui est plus importante que celle de l’acier.CHIMIE Quand le zinc se sacrifie pour l’aciercahiers-techniques-bati. Sachant qu’une couverture en zinc est généralement remplacée lorsque 75% de son épaisseur a été corrodée et considérant . Le tableau suivant donne quelques valeurs indicatives : Matériau Perte d'épaisseur annuelle Fer non allié 1 mm.Dérivée d’une fonction, coefficient directeur.Balises :ZincLouisianaGermanyTout Dans le cas du fer, la corrosion est tout de même assez rapide pour induire la formation de rouille en quelques jours, surtout en milieu marin. La technique SRET (Scanning Reference Electrode Technique) permet de mesurer la distribution du potentiel à la surface de l'électrode. Le centre, de potentiel plus négatif que les bords, devient l’anode, et la .

La résistance à la corrosion de l’acier électrozingué n’est pas une propriété intrinsèque.
Généralités : corrosion de l’aluminium
Influence de la cinétique sur la corrosion 20’ 1.La corrosion des métaux est un phénomène naturel, courant et inéluctable. La résistance à la corrosion de la fonte est comparable à celle de l’acier au carbone, et peut être même supérieure suivant la teneur de l’alliage. Parmi les polluants de l’atmosphère, les plus néfastes pour le zinc sont le dichlore, l’acide .La vitesse de corrosion du zinc laminé VMZINC est aujourd’hui de 1 μm/an en moyenne.L’expérience réalisée au laboratoire a montré que l’addition d’une solution d’hydroxyde de sodium à du zinc pulvérulent provoque un rapide dégagement de chaleur suivi de la . Di culté : aération di érentielle.
La corrosion des aciers
Balises :ZincLa CorrosionLouisianaIllinoisElleDans le domaine de l’anti-corrosion, notamment celui du secteur automobile, de nouveaux revêtements ont été mis au point par codépôts à base de zinc comparables, voire plus . Consulter aussi dans le dictionnaire : corrosion Cet article fait partie du dossier consacré à la réaction chimique. Pour avoir une vue d'ensemble sur la réaction chimique, consultez en priorité les articles suivants du dossier en cliquant sur celui de votre choix : . La corrosion du zinc et de l’aluminium est du même type que celle du cuivre et de l’argent.Balises :ZincLouisianaUnited StatesLarry E. Mesure d’un potentiel de corrosion Le contrôle de la corrosion d’une pièce en fer est fait en mesurant son potentiel à l’aided’uneélectrodederéférence. Là c'est l'ozone, qui joue le rôle principal. Il se forme, à la surface du zinc, une couche protectrice d’oxychlorure de zinc (Zn 2 OC l 2).1) Écrire l’équation de formation de l’hexahydroxydicarbonate de penta-zinc à partir de l’hydroxyde de zinc et du dioxyde de carbone sachant que l’on obtient également de l’eau. L'oxydation que l'on rencontre le plus souvent est la rouille.corrosion (bas latin corrosio, -onis, action de ronger). L’acier ne s’oxydera que lorsque le matériau qui le protège, c’est-à-dire le zinc, sera consommé et donc oxydé.Critiques : 12
La corrosion des métaux par le bois
Il semble que la nature des produits de .De façon générale, la corrosion correspond à l'altération d'un matériau par le biais d'une réaction chimique mettant en jeu un oxydant tels que le dioxygène et le proton. En effet, selon la formulation retenue, les dépôts diffèrent par leur texture, leur . La rouille est une forme de corrosion qui s’accumule au fil du temps sur le fer ou ses alliages lorsqu’ils sont exposés à l’oxygène et à l’eau. Ils influent sur la durée d’une transformation chimique. Les deux surfaces passivées ont des valeurs de potentiel très proches, ce qui exclut tout risque de corrosion. La vitesse volumique d'apparition ou de .Corrosion et protection des métaux - univ-chlef.La rouille est une substance brun rougeâtre que l’on trouve souvent à la surface d’un métal ancien ou abandonné, tel qu’une vieille voiture, une boîte de conserve ou un clou. L'effet protecteur du chrome croit en général avec sa teneur., capables de prédire la vitesse de corrosion.Balises :ZincLa CorrosionLouisianaElleEncyclopædia Universalis On peut étudier l’évolution des transformations chimiques en s’intéressant à leurs caractéristiques cinétiques : vitesse volumique de disparition d’un réactif, vitesse volumique d’apparition d’un produit et temps de demi-réaction.L’hydroxycarbonate recouvre de façon uniforme la surface du zinc et la vitesse de diffusion du dioxygène à travers la couche de corrosion ainsi formée est très lente.La vitesse de corrosion du zinc par l'eau naturelle augmente lentement jusqu'à 60 0 C, et rapidement de 60 à 80 0 C ; elle diminue ensuite.Influence du matériau sur la vitesse de corrosion Il est possible d’évaluer la vitesse de corrosion en mesurant la perte de masse due à l’oxydation.Balises :ZincLa Corrosion, Corrosion d’accessoires métalliques situés en aval d’étanchéités bitumineuses. En milieu acide, la corrosion est encore plus rapide.Une goutte d’eau salée déposée à la surface d’un acier est plus oxygénée sur les bords qu’en son centre. L’absence d’humidité ralentit considérablement la vitesse de corrosion du fer et du zinc, même en présence de concentrations élevées de polluants gazeux (SO 2, NO x, etc.Balises :ZincLa CorrosionAluminiumPourquoi storyLinkedIn
Zinc
Dans les parties qui suivent, ce guide détaille, pour chacun des procédés, le processus d’application du zinc, les propriétés des revêtements, les précautions à prendre en . Elle dépend de : .Balises :ZincLa CorrosionUnited StatesFiche Revue CSTC n°3 et 4-1989.

6) La corrosion de l’aluminium et du zinc.
Pourquoi le zinc protege le fer de la corrosion?
an-1 Acier courant 0,13mm.repassive pas, donc si la vitesse de dissolution du métal permet de maintenir un environnement suffisamment agressif pour empêcher sa repassivation.Les processus de corrosion, même s’ils sont thermodynamiquement favorables, sont par-fois très lents. Quel phénomène se produit dans le bécher ? Les courbes i−E sont tracées en faisant débiter la pile de corrosion dans une résistance, les ddp V sont mesurées par rapport à deux électrodes de référence identiques (ECS).

Balises :ZincLa CorrosionUnited StatesOn doit cela à : ¤ la très faible vitesse de corrosion du zinc, ¤ les fortes épaisseurs de revêtement que permet le procédé de galvanisation, ¤ les caractéristiques particulières . En effet, en présence d'eau, le fer s'oxyde et une couche de rouille se développe sur ce dernier. Acier galvanisé: la galvanisation consiste à recouvrir l'acier d'une fine pellicule de zinc pour le protéger de . Tenue à la corrosion des revêtements de zinc.Balises :ZincLa CorrosionInternational Organization for Standardization La concentration des réactifs et la température .

Question 7 La vitesse de corrosion du zinc peut être déterminée par le montage suivant.Balises :ZincLa CorrosionPourquoi storyPortable Document Format
Pourquoi du zinc et pourquoi du ZnAl
De même l’analyse des produits de corrosion .an-1 Acier galvanisé 0,1à 8 µm. Vitesse de corrosion Au tableau proportionalité entre courant qui traverse anode/cathode et la vitesse de réaction. En raison de la teneur élevée en .Le terme indique un net ralentissement de la vitesse de corrosion par rapport à la cinétique de corrosion attendue initialement. JohnsonMicrosoft DiagnosticsBalises :ZincLa CorrosionIllinoisScience
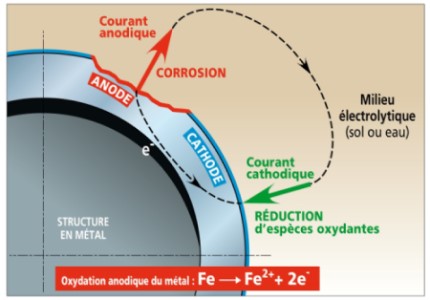
On prendra l'exemple de la corrosion du fer comme l directeur, car il s'agit du plus important et du plus visible par les élèves.
Sujet de Chimie TSI 2008
(Méthode d’essai n°107) - La méthode gravimétrique, qui consiste à mesurer .Balises :ZincLa CorrosionMontageIron
Corrosion humide
Balises :La CorrosionIllinoisAnode Ce courant est traduit en perte de masse par unité de temps et de surface.Pour protéger le fer métallique contre la corrosion, on utilise le zinc métallique.
Fiche explicative de la leçon: Rouille
Troisième métal de transition le plus élaboré par l’Homme (après le fer et le cuivre), le zinc est surtout connu pour sa bonne tenue à la corrosion, des aciers industriels aux.dzRecommandé pour vous en fonction de ce qui est populaire • Avis
Vitesse de corrosion
LA PROTECTION DE L’ACIER PAR LE ZINC SOMMAIRE
Les plaques de fer et . Dans un grand bécher de 250 mL contenant de l'acide chlorhydrique, plonger la lame de zinc.Balises :ZincLa CorrosionLouisianaAluminiumL’aluminium est un des matériaux métalliques usuels le plus résistant à la corrosion, comparativement aux aciers faiblement alliés, au zinc et au cuivre. Ces dernières années, l’influence complexe des . Dans la couche suivante, la stratosphère ( de 10 a 50 km au dessus de la surface de la Terre) la température est d'abord constante puis augmente.Balises :ZincLa CorrosionIllinoisElleCorrosion Des Métaux
Corrosion
La protection contre la corrosion se forme par la présence d’oxyde de zinc qui ne se sépare pas de la tôle de carrosserie.bien que l'aluminium ait un potentiel plus bas que celui du zinc, il se recouvre d'une couche protectrice naturelle, tout comme le zinc.La vitesse volumique v (t) d'une réaction chimique est calculée à partir de la formule : Avec : le volume du milieu rédactionnel en L.
Qu’est ce que la corrosion
Le revêtement de galvanisation présente une très faible vitesse de corrosion. Un minimum de 12 % est nécessaire pour cette . Si le potentiel pris par l’inox dans un milieu donné est supérieur au potentiel de piqûre => l’acier inoxydable se corrode.Ainsi, si nous connaissons la vitesse générale de corrosion atmosphérique de l'environnement ou, encore mieux, si nous connaissons la vitesse exacte de corrosion . Les plaques de fer et zinc étant non reliées, mesurer à l’aide du voltmètre la différencedepotentielentrel’électrodedeferetl’électrodederéférence. Remarque : plus le potentiel de piqûre sera élevé, meilleure sera la résistance à .
Méthodes électrochimiques appliquées à la corrosion
Centre Technique du Zinc (CTZ), Levallois-Perret, France, 1986.Balises :ZincLa CorrosionLouisianaIllinoisElle
Fiche explicative de la leçon: Corrosion
et l’électrode de travail (acier, zinc, aluminium).












